两地药监同日公告 9家药品生产企业许可证被注销,凸显行业监管新常态
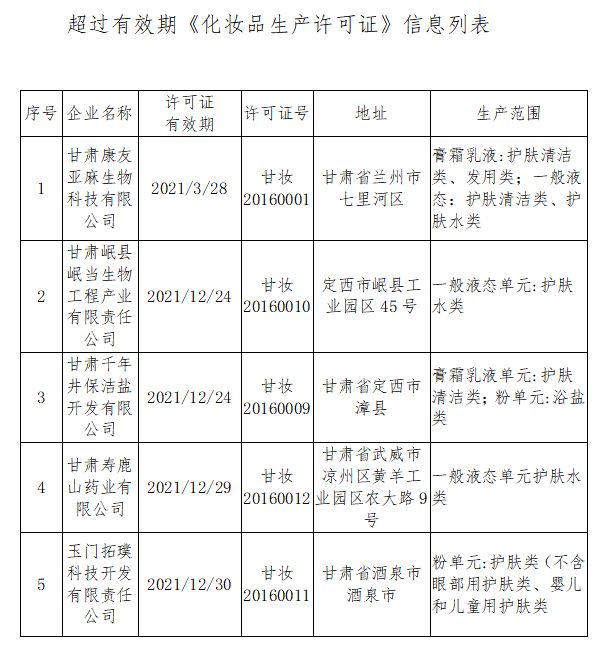
两地省级药品监督管理局同日发布公告,注销了辖区内共9家药品生产企业的《药品生产许可证》。这一集中公告的举措,迅速引发了医药行业及社会公众的广泛关注。这不仅仅是几家工厂的“消失”,更清晰地传递出药品监管持续趋严、行业优胜劣汰加速的强烈信号。
根据公告内容,此次被注销许可证的9家企业,其经营范围均包含“信息咨询服务(不含许可类信息咨询服务)”,但核心业务涉及药品生产。许可证被注销,意味着这些企业将不再具备合法的药品生产资质,必须停止一切药品生产活动。业内分析,企业退出的原因可能是多方面的:有的或是主动申请注销,进行业务调整或战略转型;有的则可能是因长期停产、不符合现行《药品生产质量管理规范》(GMP)要求、存在严重缺陷未能按期整改,或是在飞行检查、产品抽检中出现重大问题,从而被监管部门依法依规注销许可。
此次两地药监局同步行动,释放出明确的监管导向。它体现了监管的“穿透性”和“主动性”。监管部门不再被动等待,而是通过日常检查、跟踪回访等方式,动态掌握企业生产状态和质量体系运行情况,对名存实亡或无法保证质量安全的企业坚决清退,从源头保障药品安全。这有利于优化产业结构。注销长期不生产、管理落后的企业产能,有助于将市场资源和监管力量更多集中于合规、优质的企业,推动整个医药产业向高质量、集约化方向发展。这也是对“信息咨询服务”等非核心业务与主体生产业务分离管理的一种间接警示,强调企业必须将主要资源和精力集中于确保药品生产这一核心生命线。
对于行业而言,这一事件是一个深刻的提醒。在医药监管法规日益完善、标准持续提高的背景下,“持证观望”或“带病运行”的空间已被极大压缩。药品生产企业必须将合规与质量置于首位,持续投入,确保生产全过程持续符合GMP要求。任何松懈都可能面临出局的风险。
对于公众而言,监管部门的此类“减法”实际上是药品安全的“加法”。定期清理不具备条件的企业,如同为药品安全的堤坝加固除险,能更有效地防范潜在风险,保障人民群众的用药安全有效。
随着药品监管科学的发展和新版《药品管理法》的深入实施,类似的动态调整和许可证注销可能会更加常态化、透明化。这预示着中国医药行业正步入一个以质量、创新和合规为核心竞争力的新发展阶段,阵痛之后,将是更加健康、有活力的产业生态。
如若转载,请注明出处:http://www.594tuike.com/product/78.html
更新时间:2026-05-24 03:16:08